疫苗开发的监管规则在新冠疫情期间被修改,优化了开发流程。生物制药产业保留了这些变化,还是一切照“旧”?
开发和安全部署一种疫苗通常需要 5 到 10 年时间。而在新冠疫情期间,这一时间大大缩短:三种疫苗迅速获得紧急使用授权 (EUA),并在 2020 年底获得额外批准。
确保患者的安全始终是监管机构工作的重中之重。但产业界同时希望,在新冠疫情之后,监管机构可以保留疫情期间这些快速高效的监管程序。2023 年全球生物制药弹性指数调研表明,目前产业界的高级管理者对政府支持生物制药的政策和监管互动不如 2021 年乐观。新冠疫情期间,政府支持力度空前加强,现已却明显减弱,政府政策及监管弹性得分从 2021 年的 6.96 下降到 2023 年的 6.08。
监管互动需要改进
强有力的监管对于确保新药安全至关重要,但受访者建议,可以进一步提高监管互动的效率。
总体而言,在所有质量指标方面,制药公司高管可能会将其本国药品审批机构评级为“良好”。然而他们认为,开发过程中的监管互动的效率还可以进一步提高。在这方面,各国的情况各不相同,但就从申请到监管机构审批的时间(弹性报告纳入的外部指标)而言,美国和英国排名前两位。
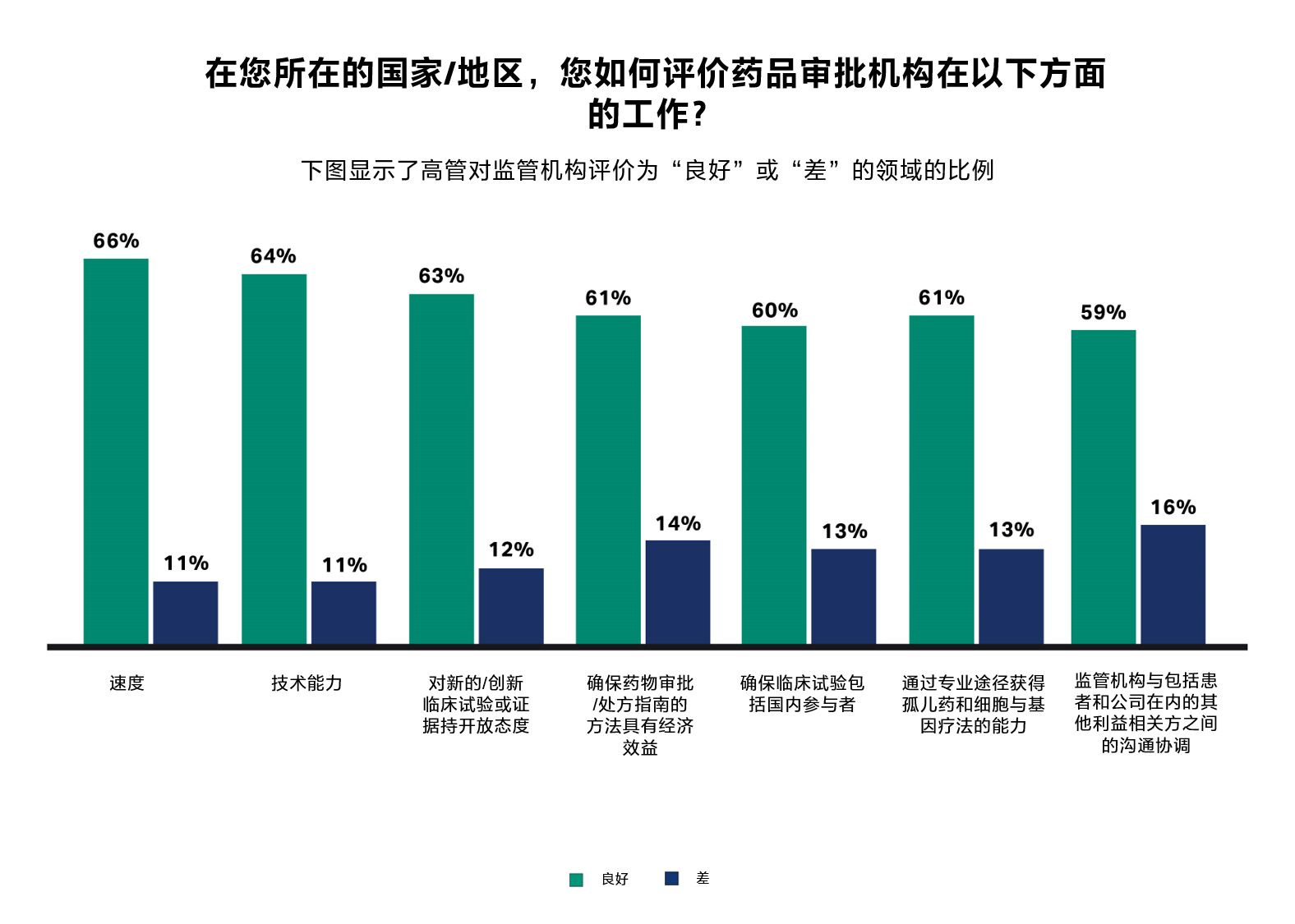 图 1.就速度、技术能力和创新开放性而言,大约三分之二的高管将其国内药品审批机构评级为“良好”。
图 1.就速度、技术能力和创新开放性而言,大约三分之二的高管将其国内药品审批机构评级为“良好”。韩国国际疫苗研究所 (IVI) 总干事 Jerome Kim 博士称,政府和产业界的监管互动不够明确。他表示:“在新冠疫情期间,采用新技术的中国疫苗获批速度不及预期,这可能也减缓了中国企业的境外审批速度,或迫使他们寻求境外审批解决方案。”但经过新冠疫情期间积累的经验,未来的药物注册和审批程序或许会受到启发。
在监管机构与生产商的互动中,让参与者有决策权至关重要。
悉尼大学临床遗传学家 Ian Alexander 说:“通常情况下,就关键决策而言,进行对话的双方往往处于食物链下游第三级。这会产生很多不确定性和挫折感,很多努力往往都是徒劳。”
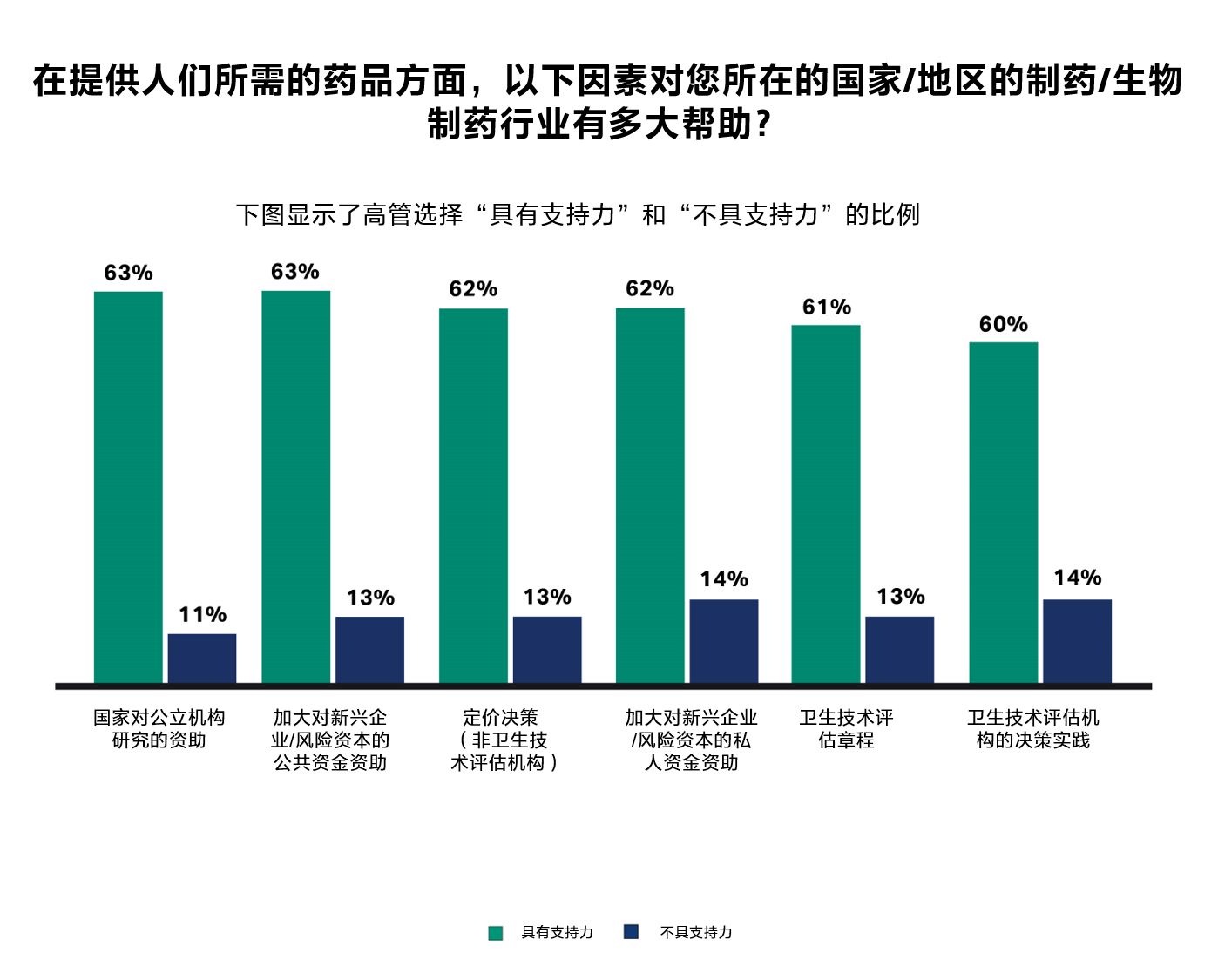 图 2.约一成受访者认为,公共和私人资金对初创企业的支持力度不足,无法帮助生物制药产业满足人们的需求。
图 2.约一成受访者认为,公共和私人资金对初创企业的支持力度不足,无法帮助生物制药产业满足人们的需求。政治和财政支持的重要性
在 2023 生物制药弹性指数的调研中,受访者对获得国家研究资助的机会更加乐观。爱尔兰国家生物工艺研究培训所 (NIBRT) 首席商务官 Killian O’Driscoll 也有同感。
他表示:“爱尔兰政府一直非常支持 NIBRT,他们最近为我们的商业案例提供了 2100 万欧元的资助,帮助我们扩建设施。大多数政府都知道生命科学产业的价值,并积极提供支持。但同样,这也因国家/地区而异。”
英国政府高价值制造弹射器计划 (HVMC) 工艺制造合作伙伴 CPI 的医药制造创新中心董事总经理 Dave Tudor 表示,除了持续投资生物制药研究、培养研究人才外,财政环境也必须宽松。
“英国需要确保为高价值制成品(此处指药品)制定有竞争力且稳定的财政政策,促进良性发展,保持竞争优势。无论是补助拨款、减免企业税或研发税,还是两者相结合,这些财政措施都需要与其他国家/地区保持一致。”
四成受访者认为,政府的激励措施对生产本土化有很大影响。但也有四成受访者认为,政府政策缺乏一致性与连贯性。例如,政策鼓励投入研发工作,但却没有为成功的开发成果定一个不错的价格;鼓励生产创新,但却没有妥善保护知识产权。这种观点在南非、日本和新加坡的受访者中尤为普遍。
总体而言,2023 年的数据表明,虽然各国政府正在采取一些措施来支持生物制药产业,但若能实施推动产业长期增长的政策,他们可以走得更长远。要成功实施这类政策,关键是要让政策制定者与生态系统中所有其他各方(包括生物制药公司管理层、专业生产商和患者组织)开展密切、有效的合作。
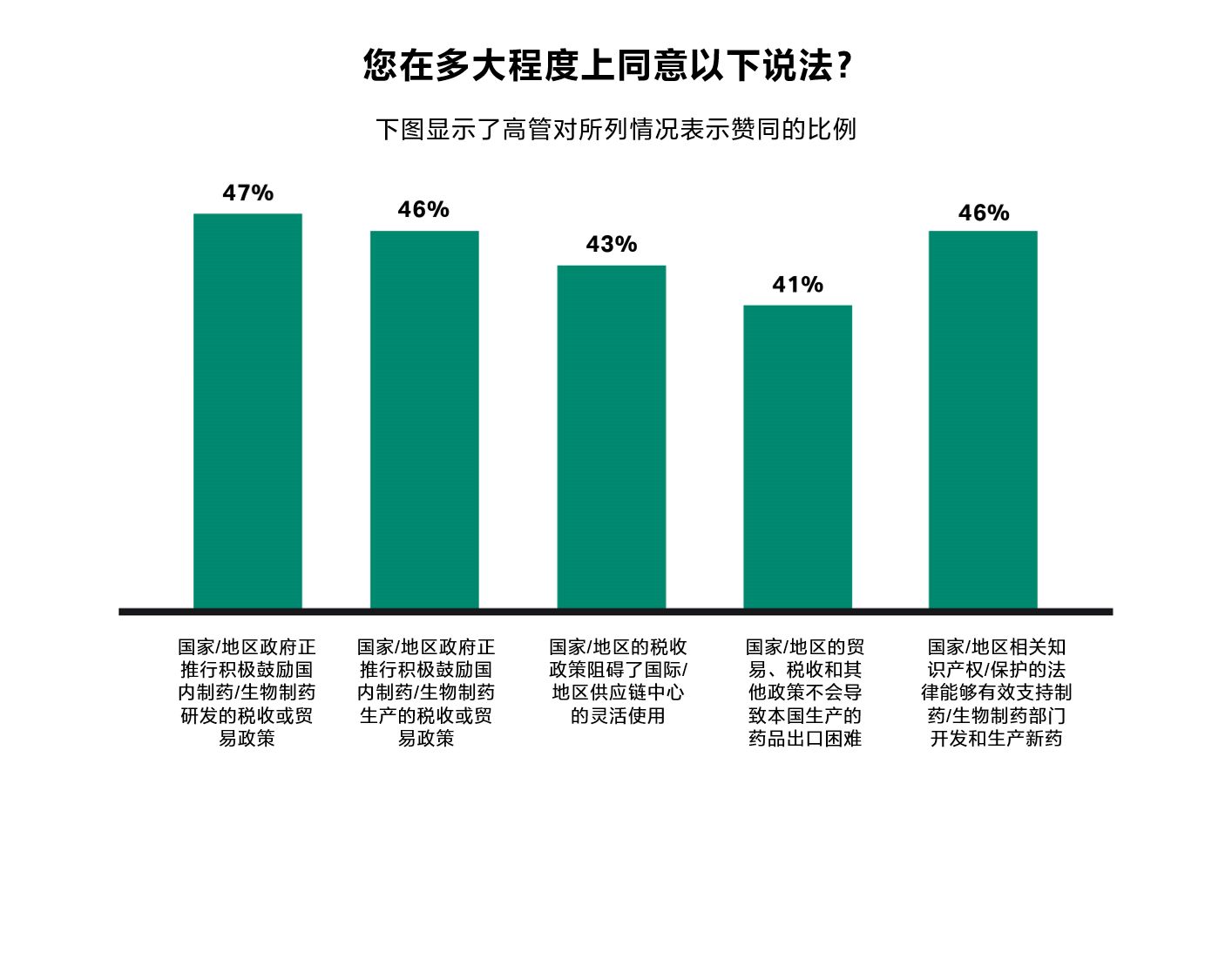 图 3.不到一半的高管认为,国内政府正在推行税收或贸易政策,积极鼓励制药/生物制药生产和研发。
图 3.不到一半的高管认为,国内政府正在推行税收或贸易政策,积极鼓励制药/生物制药生产和研发。阅读《2023 年全球生物制药弹性指数》,进一步了解政府和监管环境如何塑造全球生物制药产业的现在和未来。